فئوکروموسیتوم ها و پاراگانگلیوم ها، تومورهای مـولد کاتکولامین ها هستند که از دستگاه عصبی سمپاتیک یا پاراسمپاتیک مشتق می شوند. این تومورها ممکن است به صورت تک گیر رخ دهند یا به شکلی ارثی و بخشی از تظاهرات نئوپلازی متعدد انـدوکرین نـوع ۲ بیماری von Hippel – Lindau یا چند سندرم دیگر همراه با فئوکروموسیتوم، ایجاد شوند. تشخیص فئوکروموسیتوم ها، یکی از علل بالقوه قابل درمان هیپرتانسیون را مطرح میکند، و با خارج کردن آن ها می توان از بحران های هیپرتانسیون، که می توانند کشنده باشند، جلوگیری به عمل آورد. تظاهر بالینی این تومورها متغیر است، و از یک انسیدنتالومای فوق کلیوی، تا بیماری که به بحران هیپرتانسیون مبتلا شده و به عوارض قلبی یا عوارض عروقی مغز دچار شده است را، دربر می گیرد.
اپیدمیولوژی
برآورد می شود که سالانه از هر یک میلیون نفر، ۲ تا ۸ نفر به فئوکروموسیتوم مبتلا می شود، و حدود ۰/۱٪ از بیماران مبتلا به فشار خون، فئوکروموسیتوم دارند. سـن متوسط در هنگام تشخیص حدود ۴۰ سالگی است، هرچند که این تومورها می توانند از ابتدای کودکی تا اواخر دوران عمر بروز کنند.
مکانیسم ایجاد بیمرای در فئوکروموسیتوم
فئوکروموسیتوم ها و پاراگانگلیوم ها، تومورهای پـر عـروقی هستند که از سلول های مشتق از بافت مجاور عقده های سمپاتیک (مثل مدولای غده فوق کلیه) یا پاراسمپاتیک (مثل جسـم كـاروتید، گلوموس واگال) منشاء می گیرند. نام فئوکروموسیتوم بیانگر رنگ سیاهی است که به دلیل اکسیداسیون کرومافین کاتکولامین ها ایجاد می شود.
هرچند که اسامی مختلفی برای توصیف این تومورها به کار رفته است، ولی اکثر پزشکان از عبارت فئوکروموسیتوم برای توصیف تومورهای علامتدار مـولد کاتکولامین (از جمله تومورهایی که در مناطق خارج فـوق کلیوی خلف صـفاق، لگنی، و سینه ای واقع شـده انـد) استفاده میکنند.
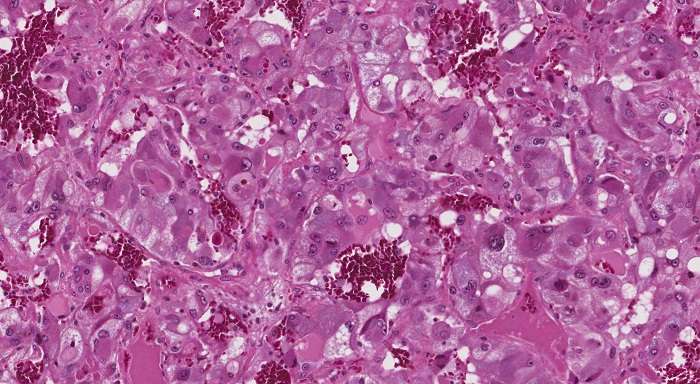
عبارت پاراگانگلیوم برای توصیف تومورهای مولد کاتکولامین در گردن و قاعده جمجمه، که ممکن است کاتکولامین اندکی ترشح کنند یا اصلا کاتکولامین ترشح نکنند، به کار می رود. در مقابل این اصطلاح شایع بالینی، WHO اصطلاح فئوکروموسیتوم را بـرای تـومورهای غـدد فوق کلیوی و اصطلاح پاراگانگلیوم را برای تومورهای دیگر مناطق به کار می برد.
علائم فئوکروموسیتوم ها
علائم فئوکروموسیتوم ها به قدری متنوع هستند که فئوکروموسیتوم را «مقلد بزرگ» نامیده اند. در میان نشانه های تظاهر این بیماری، حملات تپش قلب، سردرد، و تعریق شدید، نوعاً رخ میدهند و سه گانه کلاسیک ایـن بیماری را شامل می شوند. وجود هر سه این نشانه ها، به همراه فشار خون، احتمال تشخیص فئوکروموسیتوم را مطرح میکند. از سوی دیگر، فئوکروموسیتوم می تواند سال ها بدون علامت باشد و در برخی موارد، قبل از اینکه بیمار متوجه نشانه های بیماری شود، تومورها تا اندازه قابل توجهی رشد کرده اند.
نشـانه غـالب بیماران مبتلا به فئوکروموسیتوم ها، فشار خون است. به طور کلاسیک، بیماران به حملات فشار خون دچار می شوند، ولی فشار خون مـداوم نیز شایع است. بحران های کاتکولامینی می توانند منجر به نارسایی قلبی، ادم ریوی، آریتمی ها، و خونریزی داخل جمجمه ای شوند.
در حین حملات رهاسازی هورمون ها، که می تواند در فواصل زمانی بسیار متفاوتی رخ دهد، بیماران مضطرب و رنگ پریده هستند و دچار تاکیکاردی و تپش قلب می شوند. این حملات عموماً کمتر از یک ساعت طول می کشند و عـوامـلی کـه می توانند آنها را آشکار نمایند عبارتند از:
- جـراحی
- تغییرات وضـعیت بـدن مانند ناگهانی ایستادن از حالت خوابیده
- ورزش
- حاملگی
- ادرار کردن (بـویژه فئوکروموسیتوم های مثانه)
- و داروهـای مـختلف (مثل ضدافسردگی های سه حلقه ای، مخدرها، متوکلوپرامید).
تشخيص
تشخیص فئوکروموسیتوم بر اساس اثبات افزایش مفرط کاتکولامین با انجام آزمایش بیوشیمیایی و تعیین مـحـل تـومور از طریق تصویربرداری مسجل میشود. هر دو اقدام تشخیصی اهمیت یکسانی دارند، هرچند که به طور سنتی، اندازه گیری کاتکولامین ها یا متانفرین (متابولیت متیله کاتکولامین ها) اولین گام برای رسیدن به این تشخیص محسوب میشود.
آزمایش بیوشیمیایی تشخیص فئوکروموسیتوم ها
فئوکروموسيتوم ها و پاراگانگلیوم ها، کاتکولامین ها را، که شامل نوراپی نفرین (نورآدرنالین)، اپی نفرین (آدرنالین)، و دوپامین هستند، سنتز و ذخیره می کنند. افـزایش سطوح پلاسمایی و ادراری کاتکولامین ها و متانفرین ها، سنگ بنای تشخیص این بیماری به شمار می روند.
فعالیت هورمونی تومورها متغیر است، و لذا تنوع قابل ملاحظه ای در نتایج اندازه گیری های پیاپی کاتکولامین ها مشاهده می شود. با ایـن حـال متابولیتهای O متیله به طور مداوم از اکثر تومورها نشت میکنند، و با اندازه گیری متانفرین ها زمانی که این مقادیر به ۳ برابر بیشترین حد طبیعی افزایش یافته باشند، صـرف نظر از روش سنجش بکار رفته، تشخیص فئوکروموسیتوم بسیار محتمل است.
اندازه گیری متانفرین های پلاسما، حساسترین روش است و کمتر در معرض افزایش مثبت کاذب ناشی از استرس از جمله استرس مربوط به خونگیری قرار میگیرد. هرچند که با معرفی روش های سنجش جدید، بروز نتایج مثبت کاذب کاهش یافته است، ولی پاسخ های فیزیولوژیک به استرس و همچنین داروهایی که کاتکولامین ها را افزایش می دهند، هنوز هم می توانند این آزمایشات را مخدوش نمایند.
از آنجا که این تومورها نسبتاً نادر هستند، افزایش های بینابینی احتمالاً نتایج مثبت کاذب را نشان میدهند. در این شرایط، کنارگذاشتن رژیم غذایی یا مصرف داروهایی (قطع مصرف لوودوپا، داروهای مقلد اثرات سمپاتیک، داروهـای مـدر، داروهای ضد افسردگی سه حلقه ای، داروهای مسدودکننده گیرنده های آلفا و بتا) که ممکن است نتایج مثبت کاذب ایجاد کنند و سپس تکرار آزمایش یا انجام آزمون سرکوب کلونیدین (اندازه گیری سطح پلاسمایی متانفرین ۳ ساعت مصرف خوراکی ۳۰۰ میکروگرم کلونیدین) حائز اهمیت میباشد.
سایر آزمایشهای دارویی، نظیر آزمایش فنتولامین و تست تحریکی گلوکاگون، حساسیت نسبتاً پایینی دارند و توصیه نمی شوند.
تصویربرداری تشخیصی
روش های مختلفی بـرای تعیین محل فئوکروموسیتوم ها و پاراگانگلیوم ها به کار رفته اند. CT و MRI حساسیت مشابهی دارند. CT باید با ماده حاجب انجام شود. MRI بر پایه T2 همراه با ماده حاجب گادولینیوم، برای شناسایی فئوکروموسیتوم ها روش بهینه است و بـرای تصویربرداری از پاراگانگلیوم ها و فئوکروموسیتوم های خارج از غده فوق کلیوی، تا حدودی از CT بهتر است. حدود ۵٪ از انسیدنتالوم های فوق کلیوی، که معمولاً با CT یا MRI شناسایی می شوند، پس از ارزیابی اندوکرینولوژیک، فئوکروموسیتوم تشخیص داده می شوند.
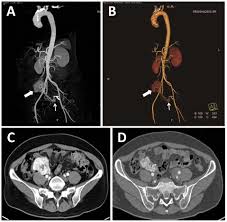
برای تعیین محل تومورها همچنین می توان از ردیابی مواد نشاندار رادیواکتیو، نظیر سینتی گرافی، ۱۳۱۱ یا ۱۲۳۱ متایدوبنزیل گوانیدین (MIBG)، آنالوگ های سوماتواستاتین ۱۱۱In توموگرافی گسیل پوزیترون با ۱۸F-DOPA، یا توموگرافی گسیل پوزیترون با FDG که ممکن است با برداشتن کامل یا قسمتی از غده فوق کلیوی بدان دست یافت استفاده کرد. از آنجا که این مواد در پاراگانگلیوم ها به صورت انتخابی برداشت می شوند، تصویربرداری هسته ای به ویژه در سندرم های ارثی مفید است.
درمان فئوکروموسیتوم
خارج کردن کامل تومور، هدف نهایی درمان فئوکروموسیتوم است. حفظ بافت طبیعی قشر غده فوق کلیه (به ویژه در اختلالات ارثی که به احتامل زیاد فئوکروموسیتوم دوطرفه است) اهمیت به سزایی دارد. برای اینکه عمل جراحی بدون خطر انجام شود، آماده سازی بیمار قبل از جراحی ضروری است.
قبل از عمل جراحی، فشار خون باید به طور ثابت کمتر از ۱۶۰/۹۰ حفظ شود. به طور کلاسیک فشار خون به وسیله آلفا بلاکرها کنترل می شود (۰۰/۵ تا ۴mg فنوکسی بنزامین خوراکی به ازای هر kg وزن بدن). از آنجا که بیماران دچار کمبود حجم داخل عروقی هستند، مصرف آزادانه نمک و مایعات برای اجتناب از افت وضعیتی فشار خون ضروری است.
در زمانی که منتظر تأثیرگذاری کافی آلفا بلاکرها هستیم می توان برای جلوگیری از حملات افزایش فشار خون از پرازوسین خوراکی یا فنتولامين وریدی استفاده کرد. از سایر داروهـای ضـد هیپرتانسیون، نظیر مسدودکننده های کانال کلسیم یا مهارکننده های آنزیم مبدل آنژیوتانسین، نیز به نحو موثری استفاده شده است. عمل جـراحی می بایست توسط گروهی متشکل از متخصصین بیهوشی و جـــراحـی کـه در خارج سازی فئوکروموسیتوم ها تجربه داشته باشند، انجام شود. در طول جراحی، به ویژه در شروع لوله گذاری نای یا هنگام دستکاری تومور، ممکن است نوسان فشار خون رخ دهد. انفوزیون نیتروپروساید بـرای بـحـران های نامتناسب هیپرتانسیون در حین جراحی مفید است، و افت فشار خون معمولاً به انفوزیون مایعات پاسخ میدهد.
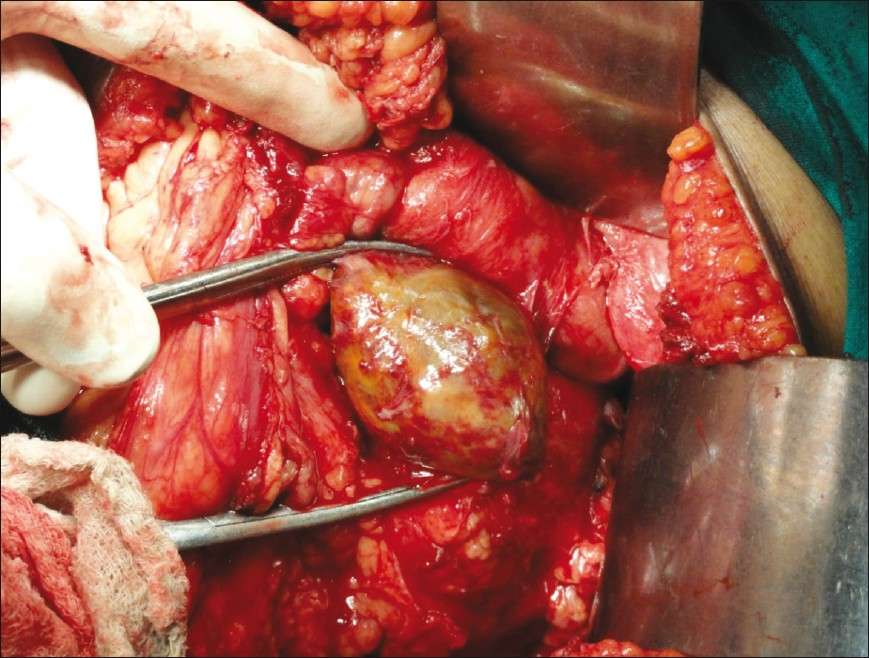
تکنیک های بـا حـداقـل تـهاجم (لاپاروسکوپی و رتروپریتوئنوسکوپی) امروزه به روش جراحی استاندارد برای فتوکروموسیتوم تبدیل شده اند. در این روش ها عوارض کمتر است، زخم جـراحی ظاهر زیباتری دارد و طـول مـدت بهبودی پس از جـراحـی نیز کوتاه تر است. فئوکروموسیتوم های شکمی خارج از غده فوق کلیوی و همچنین اکثر فئوکروموسیتوم های درون قفسه سینه را نیز میتوان بوسیله آندوسکوپی خارج کرد. پس از جراحی، باید طبیعی شدن کاتکولامین ها را اثبات کرد. پس از انجام جراحی دوطرفه با حفظ قشر غدد فوق کلیوی، برای بررسی و رد کردن کمبود کورتیزول، باید آزمایش هورمون آدرنوکورتیکوتروپ انجام شود.
فئوکروموسیتوم بدخیم
حدود ۵ تا ۱۰٪ از فئوکروموسیتوم ها و پاراگانگلیوم ها، بدخیم هستند. تشخیص فئوکروموسیتوم بدخیم، مشکل است. معیارهای معمول بافت شناسی مثل آتیپی سلولی، وجـود میتوز، و تهاجم به عروق یا بافتهای مجاور، برای تشخیص فئـوکروموسیتوم کـافی نیستند. بنابراین، اصطلاح فئوکروموسیتوم بدخیم عموماً منحصر به تومورهایی می شود که متاستاز دوردست داده اند؛ شایعترین مکان های این متاستازها، که به کمک تصویربرداری هسته ای یافت میشوند، عبارتند از:
- ریه ها
- استخوان
- کبد
که مسیر عروقی انتشار این تومور را مطرح میکنند. از آنجا که سندرم های ارثی با تومورهای چند کانونی در جایگاه های متعدد همراهند، این ویژگی ها را باید در بیماران مبتلا به جهش های رده زایا در ژنهای SDHD ،WHL RET یا SDHB، انتظار داشت. در این سندرم ها، به ویژه در حاملین جهش های SDHB، نیز متاستازهای دوردست رخ میدهند.
درمـان فـئوکروموسیتوم بـدخیم، چالش برانگیز است. روش های ممکن عبارتند از: کاهش توده تومور؛ تجویز مسدود کننده های گیرنده آلفا برای رفع علائم؛ شیمی درمانی؛ و پرتودرمانی طب هسته ای.
فئوکروموسیتوم در حاملگی
فئوکروموسیتوم گاه در طول حاملگی تشخیص داده میشود. خارج سازی بوسیله آندوسکوپی، ترجیحاً در ماه های چهارم تا ششم حاملگی، امکان پذیر است و می تواند با زایمان بدون مشكـل هـمراه باشد. غربالگری منظم خانواده هایی که فتوکروموسیتوم ارثی در آنها وجود دارد، فرصتی بـرای شناسایی و خارج کردن تومورهای بدون علامت در زنان در سنین باروری فراهم می آورد.